 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知反应在298K时=-128.0kJ·mol-1,试计算298K时的。
已知反应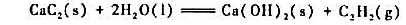
在298K时=-128.0kJ·mol-1,试计算298K时的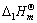 。
。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应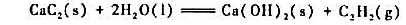
在298K时=-128.0kJ·mol-1,试计算298K时的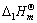 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应在298K时=-128.0kJ·mol-1,试计算2…”相关的问题
更多“已知反应在298K时=-128.0kJ·mol-1,试计算2…”相关的问题
已知在定温(298K)、定压(101325pa)下,

试确定下列反应的热效应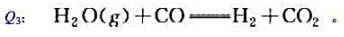 并计算该反应在2000K时的热效应.
并计算该反应在2000K时的热效应.
298K,标准状态下,利用热力学数据求算下列反应的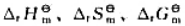 ,并根据求得数据说明,此反应在净化汽车尾气中的NO和CO时,在理论上的可能性。
,并根据求得数据说明,此反应在净化汽车尾气中的NO和CO时,在理论上的可能性。
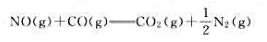
已知电极反应:
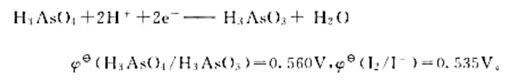
计算下列反应:
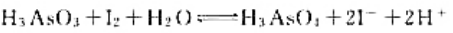
(1)在298K时的平衡常数;
(2)如果pH=7,其他物质浓度均为标准态,反应向什么方向进行?
(3)如果溶液的c(H+)=6.0mol·L-1.其他物质浓度均为标准态.反应向什么方向进行?
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变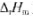 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
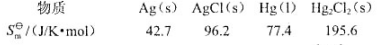 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数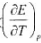
已知反应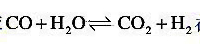 在700K时的平衡常数Kp=9,反应开始时系统中含有H2O、CO2、H2各1kmol,试求平衡组成.
在700K时的平衡常数Kp=9,反应开始时系统中含有H2O、CO2、H2各1kmol,试求平衡组成.
298K时,已知 =0.799V,
=0.799V, =0.373V,试计算Ag(NH3)2;的络合平衡常数
=0.373V,试计算Ag(NH3)2;的络合平衡常数
用标准摩尔吉布斯自由能雨数及标准摩尔焓函数计算下列合成氨反应在1000K时
的标准平衡常数.
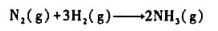
已知数据如下:

A.v=kc2(CH3COCH3)c(H+)
B.v=kc(CH3COCH3)c(H+)
C.v=kc(CH3COCH3)c(l2)
D.v=kc(CH3COCH3)c2(l2)