 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在大气中可以发生下列反应:计算上述各反应的ΔrHθm(298K).
在大气中可以发生下列反应:

计算上述各反应的ΔrHθm(298K).
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在大气中可以发生下列反应:

计算上述各反应的ΔrHθm(298K).
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在大气中可以发生下列反应:计算上述各反应的ΔrHθm(298…”相关的问题
更多“在大气中可以发生下列反应:计算上述各反应的ΔrHθm(298…”相关的问题
已知下列各反应298K时的自由能改变量:
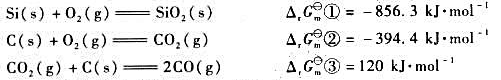
(1)试通过计算说明,制备单质Si的反应:
SiO2(s)+2C(s)=Si(s)+2CO(g)
在常温下不能自发进行。
(2)查热力学数据表,计算上述制备反应的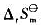 ,进一步计算该反应进行的最低温度要求。
,进一步计算该反应进行的最低温度要求。
(1)根据电极点位表数据计算反应:
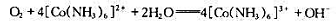
的平衡常数K.
(2)现将空气(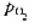 =20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
=20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
[Co(NH3)6]3+,2.0mol·dm-3NH2+及2.0mol·dm-3NH3·H2O的混合溶液中,能否发生上述反应?
A.火山爆发喷出的二氧化硫与大气中的氧结合会形成硫酸雾或硫酸盐气溶胶,引起环境酸化,后者还会通过直接或间接辐射强迫作用影响气候变化
B.颗粒物质是漂浮在大气中的固体和液体微粒,颗粒物质能散射和吸收阳光,使可见度降低,影响交通,增加汽车与航空事故
C.工业生产排放出的氮氧化物和乙醛会发生光化学反应生成过氧乙酰硫酸酯,该物质强烈刺激眼睛,会引起呼吸困难、心功能障碍和肺功能衰竭等一系列症状
D.汽车发动机排放的污染物中的氮氧化物和碳氢化合物,经阳光照射,在大气中形成光化学烟雾,对人类呼吸系统产生极大危害
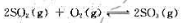
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
已知下列原电池:
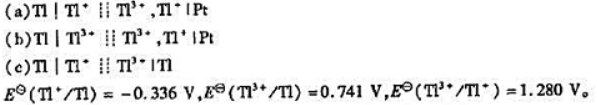
(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;
(2)计算各电池的标准电动势EθMP;
(3)计算各电池反应的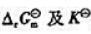 .
.
化学反应如下:
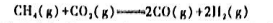
(1)利用教材附录中各物质的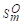 ,Δt
,Δt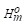 数据,求上述反应在25℃时的
数据,求上述反应在25℃时的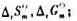
(2)利用教材附录中各物质的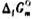 数据,计算上述及应在25℃时的
数据,计算上述及应在25℃时的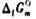 ;
;
(3)25℃,若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的ΔtSm,ΔtGm.
下面哪项最能加强上述的论述?
A.人们无法准确测出作为冰箱制冷剂存在的破坏臭氧层的化学物质的数量
B.在现代社会,为避免不健康甚至对生命构成潜在威胁的状况,冷藏食物是必要的
C.即使人们放弃使用冰箱,早已存在于冰箱中的制冷剂还是会威胁大气中的臭氧
D.冰箱中的制冷剂可以在冰箱完成使命后被完全开发并重新使用
利用标准摩尔生成炕数据计算下列反应的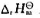 及
及 假定反应中的各气体都可视作理想气体。
假定反应中的各气体都可视作理想气体。
(1)H2S(g)+O2(g)=H2O(1)+SO2(g)
(2)CO(g)+2H2(g)=CH3OH(1)
已知298.15K时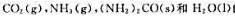 的标准摩尔生成焓和标准摩尔熵如下表所示:
的标准摩尔生成焓和标准摩尔熵如下表所示:

试通过计算判断下列反应
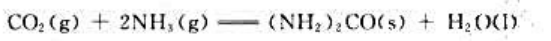
在298.15K、标准状态下能否自发进行。上述反应在标准状态下自发进行的最高温度是多少?