 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
298.15K时,已知AgCl在纯水中的溶解度1.33×10-5mol·L-1,计算AgCl在0.01mol·L-1
NaCl溶液中的溶解度。已知AgCl的Kθsp=1.77X1010.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298.15K时,已知AgCl在纯水中的溶解度1.33×10…”相关的问题
更多“298.15K时,已知AgCl在纯水中的溶解度1.33×10…”相关的问题
A.大
B.小
C.相等
D.2倍
已知298.15K时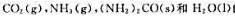 的标准摩尔生成焓和标准摩尔熵如下表所示:
的标准摩尔生成焓和标准摩尔熵如下表所示:

试通过计算判断下列反应
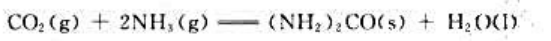
在298.15K、标准状态下能否自发进行。上述反应在标准状态下自发进行的最高温度是多少?
已知25°C时水的离子积KW=1.008x10-14,NaOH,HCI和NaCl的Amm分别等于0.024811S.m2·mol-1.0.042616S.m2.mol-1和0.012645S.m2.mol-1.
(1)求25°C时纯水的电导率;
(2)利用上述纯水配制AgBr饱和水溶液,测得溶液的电导率k(溶液)=1.664x10-5S.m-1,求AgBr(s)在纯水中的溶解度.
298.15K时,已知下列热化学方程式
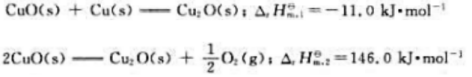
则298.15K时,CuO(s)的标准摩尔生成焓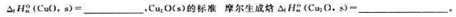
已知25℃时AgCl(s);水溶液中Ag+,CI-的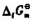 分别为-109.789kJ·mol-1,
分别为-109.789kJ·mol-1,
77.107kJ·mol-1和-131.228kJ·mol-1.求25℃下AgCl(s)在水溶液的标准溶度积Kθ及溶解度s.