 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用教材附表中的数据,计算298K下反应:的标准平衡常数.
用教材附表中的数据,计算298K下反应: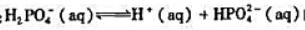 的标准平衡常数.
的标准平衡常数.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用教材附表中的数据,计算298K下反应: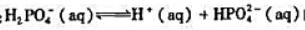 的标准平衡常数.
的标准平衡常数.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用教材附表中的数据,计算298K下反应:的标准平衡常数.”相关的问题
更多“用教材附表中的数据,计算298K下反应:的标准平衡常数.”相关的问题
查表列出298K时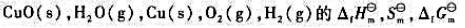 等热力学数据,试据此计算下列反应298K时的
等热力学数据,试据此计算下列反应298K时的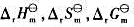 和1000K时的
和1000K时的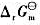 ,并进一步讨论反应的逆转温度。
,并进一步讨论反应的逆转温度。
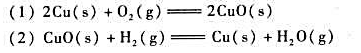
(1)计算298K下反应: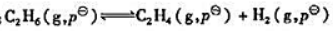 的
的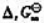 并判断在标准状态下反应向何方进行.
并判断在标准状态下反应向何方进行.
(2)计算298K反应: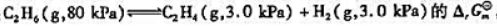 并判断反应方向.
并判断反应方向.
已知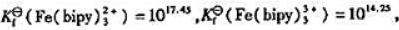 其他数据查附表.
其他数据查附表.
(1)计算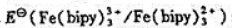 ;
;
(2)将Cl2(g)通入[Fe(bipy)3]2+溶液中,Cl2能否将其氧化?写出反应方程式,并计算25℃下该反应的标准平衡常数Kθ;
(3)若溶液中[Fe(bipy)3]2+的依度为0.20mol·L-1,所通Cl2的压力始终保持100.0KθPa,求平衡时溶液中各离子浓度.
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变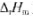 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
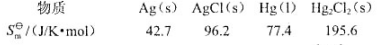 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数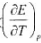
已知在定温(298K)、定压(101325pa)下,

试确定下列反应的热效应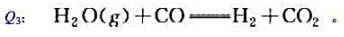 并计算该反应在2000K时的热效应.
并计算该反应在2000K时的热效应.
料.它们的燃烧反应分别为
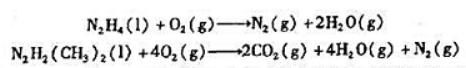
通过计算比较每克联氨和二甲基联氨燃烧时,何者放出的热量多(已知ΔH(N2H3(CH3)2),l)=
42.0kJ·mol-1,其余所得数据由附表中自已查出).
在大气中可以发生下列反应:

计算上述各反应的ΔrHθm(298K).
化学反应如下:
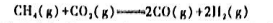
(1)利用教材附录中各物质的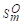 ,Δt
,Δt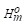 数据,求上述反应在25℃时的
数据,求上述反应在25℃时的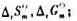
(2)利用教材附录中各物质的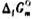 数据,计算上述及应在25℃时的
数据,计算上述及应在25℃时的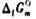 ;
;
(3)25℃,若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的ΔtSm,ΔtGm.
已知反应:

298K时的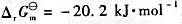 。试计算:
。试计算:
(1)该反应的标准平衡常数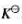 ;
;
(2)若空气中H2S的分压为3.1Pa,试计算可以确保铜单质免遭H2S腐蚀时H2的分压。