 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
设温度为T时,A、B两液体的饱和蒸气压分别为pA*,pB*,且pA*>pB*。A、B两液体混合成理想液态混合物,当气相中的yA=0.5时,液相中的组成为()。
A.xA<xB
B.xA >xB
C.xA=xB
D.不能确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.xA<xB
B.xA >xB
C.xA=xB
D.不能确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“设温度为T时,A、B两液体的饱和蒸气压分别为pA*,pB*,…”相关的问题
更多“设温度为T时,A、B两液体的饱和蒸气压分别为pA*,pB*,…”相关的问题
温度T下,A,B两组分液态完全互溶,其饱和蒸气压分别为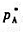 和
和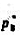 ,且
,且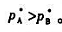 .在A,B组成的气-液平衡系统中,当系统组成xB<0.3.时,向系统中加入B(I)会使系统压力增大;当系统组成xB>0.3时,向系统中加入B(I)则系统压力降低,则该系统具有()恒沸点.
.在A,B组成的气-液平衡系统中,当系统组成xB<0.3.时,向系统中加入B(I)会使系统压力增大;当系统组成xB>0.3时,向系统中加入B(I)则系统压力降低,则该系统具有()恒沸点.
已知液体甲苯(A)和液体苯(B)在90°C时的饱和蒸气压分别为PA’=54.22cPa和PB’=136.12KPa.两者可形成理想液态混合物。今有系统组成为xB.O=0.3的甲苯苯混合物5mol,在90°C下成气-液两相平衡,若气相组成为yB=0.4556求:
(1)平衡时液相组成石及系统的压力P。
(2)平衡时气、液两相的物质的量n(g),n(l)
已知在100kPa下水的凝固点为0℃,在-5℃时,过冷水的比凝固焓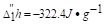 ,过冷水和冰的饱和蒸气压分别为p"(H2O,l)=0.422kPa及p"(H2O,s)=0.414kPa.今在100kPa下,有-5℃,1kg的过冷水变为同样温度、压力下的冰,设计可逆途径,分别按可逆途径计算过程的ΔS及ΔG.
,过冷水和冰的饱和蒸气压分别为p"(H2O,l)=0.422kPa及p"(H2O,s)=0.414kPa.今在100kPa下,有-5℃,1kg的过冷水变为同样温度、压力下的冰,设计可逆途径,分别按可逆途径计算过程的ΔS及ΔG.
A.37.5
B.21.5
C.8.0
D.29.5
已知在100kPa下水的凝固点为0°C,在-5°C,过冷水的比凝固焓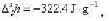 过冷水和冰的饱和蒸气压分别为
过冷水和冰的饱和蒸气压分别为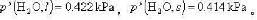 今在100kPa下,有-5°C1kg的过冷水变为同样温度、压力下的冰,设计可逆途径,分别按可逆途径计算过程的ΔS及ΔG.
今在100kPa下,有-5°C1kg的过冷水变为同样温度、压力下的冰,设计可逆途径,分别按可逆途径计算过程的ΔS及ΔG.
A.等于0.5
B.小于0.5
C.大于0.5
D.无法确定
反应A+2B→D的速率方程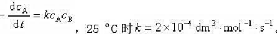
(1)若初始溶度cA,O=0.02md·dm-3,cB,O=0.04mol·dm-3,求t1。
(2)若将反应物A与B的挥发性固体装入5dm3密闭容器中,已知25°C时A和B的饱和蒸气压分别为10kPa和2kPa,问25°C时0.5molA转化为产物需多长时间?