 更多“ 硅和氧很容易化合成二氧化硅,所以硅铁常用于炼钢作()。”相关的问题
更多“ 硅和氧很容易化合成二氧化硅,所以硅铁常用于炼钢作()。”相关的问题
简要回答下列问题:
(1)拟将下列离子转化为碳酸正盐,试说明怎样选择沉淀剂,并写出反应方程式:
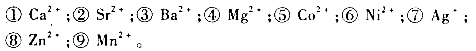
(2)从二氧化硅氯化制备SiCl4,需要和焦炭共热进行反应的耦合:
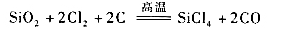
而用HF对二氧化硅进行氟化制备SiF4则不需要反应的耦合:
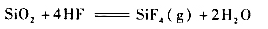
(3)Pb与稀盐酸反应,速率很慢且反应会停止;但与浓盐酸作用时,反应容易进行。试给出合理解释。
(4)从H3BO3显酸性的机理去说明为什么H3BO3是一元弱酸。
(5)试解释下列无机含氧酸的氧化性由强到弱的原因:
HClO4>H2SO4>H3PO4>H2SiO3
(6)为什么硅不与氧化性酸反应,但又可溶于HNO3及HF混合溶液中?
(7)用平面图示的方法表示单聚硅酸根SiO44-,焦硅酸根Si2O74-,链三聚硅酸根和环六聚硅酸根。写出链n聚和环n聚多硅酸根的化学式。
(8)画简图表示乙硼烷的结构,并说明其中3中心2电子键的形成过程。
(9)硼砂Na2[B4O5(OH)4]·8H2O是四硼酸的钠盐。试说明通常将硼砂的化学式写成Na2B4O7原因。为什么硼砂溶于水形成缓冲溶液?试计算其pH。
(10)三氟化硼分子是单聚体BF3,同样属于缺电子结构的乙硼烷分子却是B2H6。或者说是二聚的BH3。从结构角度如何解释这种现象?
(11)BiI5和PbI4均不能稳定存在,却有TU3存在,试说明其原因。
(12)试比较乙硼烷、烷烃、甲硅烷三者的热稳定性,写出其受热分解的化学反应方程式。
合成与制备:
(1)FeCl3催化氯化二硫化碳制备四氯化碳;
(2)用化学反应方程式表示以SiO2为原料生产粗硅,再经提纯得到纯硅的过程;
(3)用化学反应方程式表示以二氧化硅为原料制备甲硅烷及制备纯的甲硅烷的过程;
(4)以硼砂为原料制取B2O3;
(5)以方铅矿(PbS)为原料制备二氧化铅;
(6)如何以二氧化硅为原料制备水玻璃?
(7)如何以水玻璃为原料制备变色硅胶?
(8)如何配制SnCl2溶液?
A.某种溶液的导电性能不如金属,又不是绝缘体,所以,这种溶液是半导体
B.汞的导电性大大小于铝.铜.铁等金属材料,所以,汞是半导体物质
C.干燥的木块不导电,将木块弄潮湿后开始导电,但导电性能远不如铝.铜等金属材料,有人说,“潮湿将木块由绝缘体变为半导体”的说法是错误的
D.在纯结晶状态的硅中掺入某些元素原子后,会由不导电变为导电,但它在某一个方向导电比另一个方向容易些,而且导电能力受电压等外界因素影响大。这些导电性能不如金属,
所以,硅是半导体物质
A.某溶液的导电性能不如金属,又不是绝缘体。所以这种溶液是半导体
B.干燥的木块不导电,将木块弄潮湿后开始导电,但导电性能远不如铝、铜等金属。因此,“潮湿将木块由绝缘体变为半导体”的说法是错误的
C.汞的导电性大大小于铝、铜、铁等金属材料,所以,汞是半导体物质
D.在纯结晶状态的硅中掺入某些元素原子后,会由不导电变为导电,但它在某一个方向导电比另一个方向容易些,而且导电能力受电压等外界因素影响大。这些导电性能不如金属,所以,是硅半导体物质
半导体是导电性介于金属和绝缘体之间的物质。
按这个定义,下面说法错误的是()。
A. 某种溶液的导电性能不如金属,又不是绝缘体,所以,这种溶液是半导体
B. 汞的导电性能大大小于铝、铜、铁等金属材料,所以汞是半导体物质
C. 干燥的木块不导电,将木块弄潮湿后开始导电,但导电性能远不如铝、铜、等金属材料。有人说,“潮湿将木块由绝缘体变为半导体”的说法是错误的
D. 在纯结晶状态的硅中掺入某些元素原子后,会由不导电变为导电。但它在某一个方向导电比另一个方向容易些,而且导电能力受电压等外界因素影响大。这些导电性能不如金属,所以,硅是半导体物质


 如果结果不匹配,请
如果结果不匹配,请 

















