题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
温度为T的某抽空容器中,NH4HCO(s)发生下列分解反应:反应达到平衡时,气体的总压力为60kPa,
温度为T的某抽空容器中,NH4HCO(s)发生下列分解反应:
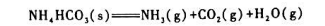
反应达到平衡时,气体的总压力为60kPa,则此反应的标准平衡常数Kθ=().
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
温度为T的某抽空容器中,NH4HCO(s)发生下列分解反应:
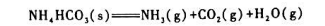
反应达到平衡时,气体的总压力为60kPa,则此反应的标准平衡常数Kθ=().
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“温度为T的某抽空容器中,NH4HCO(s)发生下列分解反应:…”相关的问题
更多“温度为T的某抽空容器中,NH4HCO(s)发生下列分解反应:…”相关的问题
A.0.0627
B.0.1026
C.0.1354
D.0.0513
,此时系统的平衡压力为104.67kPa.在同样的条件下,若放人的是NH4I(s),则测得的平衡压力为18.864kPa,试求当NH4CI(s)和NH4I(s)同时存在时,反应系统在340℃下达平衡时的总压.设HI(g)不分解,且此两种盐类不形成固溶体.
在一个抽空的容器中,放入过量的NHI(s)并发生下列反应:
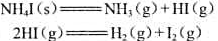 系统的相数φ=();组分数K=(); 自由度f=()。
系统的相数φ=();组分数K=(); 自由度f=()。
(s).现将隔板撤掉,整个系统达到热平衡,求末态温度t及过程的△H.已知:Ar(g)和Cu(s)的摩尔定压热容Cp,m分别为20.786J·mol-1·K-1及24.435J·mol-1·K-1,且假设均不随温度而变化.
现将隔板撤掉,整个系统达到热平衡,求末态温度t及过程的ΔH.已知:Ar(g)和Cu(s)的摩尔定压热容Cp·m分别为20.786J·mol-1·K-1及24.435J·mol-1·K-1,且假设均不随温度而变。
指出下列平衡系统中的组分数C,相数P及自由度F.
(1)l2(s)与其蒸气成平衡:
(2)MgCO3(s)与其分解产物MgO(s)和CO2(g)成平衡;
(3)NH4CI(s)放入一抽空的容器中,与其分解产物NH3(g)和HCI(g)成平衡;
(4)任意量的NH3(g)和H2S(g)与NH4HS(s)成平衡;
(5)过量的NH4HCO3(s)与其分解产物NH3(g),H2O(g)和CO2(g)成平衡;
(6)I2作为溶质在两不互溶液体H2O和CCI4中达到分配平衡(凝聚系统).
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的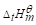
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
A.125kPa
B.120kPa
C.180kPa
D.75kPa