 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知M2+离子3d轨道中有5个d电子,请推出:(1)M原子的核外电子排布式;(2)M原子的最外层和最高能级组中电子数;(3)M元素在周期表中的位置。
已知M2+离子3d轨道中有5个d电子,请推出:(1)M原子的核外电子排布式;(2)M原子的最外层和最高能级组中电子数;(3)M元素在周期表中的位置。
此题为判断题(对,错)。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
此题为判断题(对,错)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知M2+离子3d轨道中有5个d电子,请推出:(1)M原子的…”相关的问题
更多“已知M2+离子3d轨道中有5个d电子,请推出:(1)M原子的…”相关的问题
符合下列每一种情况的各是哪一族或哪一种元素?
①最外层有6个p电子.
②+3价离子的电子构型与氩原子实[Ar]相同。
③3d轨道全充满,4s轨道只有1个电子。
①电负性相差最大的两种元素。
③在n=4,l=0轨道上的两个电子和n=3,l=2轨道上的5个电子是价电子
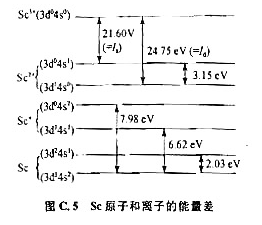
图C.5列出Sc原子和离子的能量差,请回答或据此解答下列问题:
(1)Sc原子的3d和4s电子结合能;
(2)Sc原子的电子互斥能J(s,s),J(d,s)和J(d,d);
(3)Sc原子的3d和4s单电子轨道能;
(4)讨论价电子的增填次序和电离次序。
和t2g轨道中的分布,并估计它们的磁矩各约为多少(B.M.).指出这些配合物中何者为商自旋排布,何者为低自旋排布.
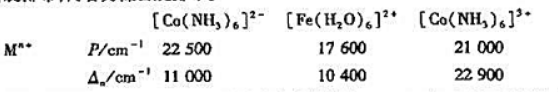
已知[Co(NH3)6]2+的磁矩为4.2B.M.,按价键理论该配离子的轨道杂化类型为________,空间构型为________ ,价层电子分布为________。
A.M2+的离子半径比N2- 小
B.M的原子序数比N小
C.M和N原子的电子层数相同
D.M和N原子最外层电子数相同
下列说法正确的是()。
A.任何原子中,d轨道能量总比s轨道能量高
B.主量子数为3时,有3s,3p,3d共3个轨道
C.除氢原子外的其他原子,3p轨道的能量总比3s轨道能量高
D.s电子在核外沿着球形轨道运动