 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
精密称取某铝盐试样0.3742g,加入EDTA标准溶液(0.05100mol/L)25.00ml,过量的EDTA溶液用锌标准溶液(0.04728mol/L)回滴,用去14.08ml。求试样中铝的百分含量。(MAl=26.98)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“精密称取某铝盐试样0.3742g,加入EDTA标准溶液(0.…”相关的问题
更多“精密称取某铝盐试样0.3742g,加入EDTA标准溶液(0.…”相关的问题
称取含铝试样1.000g,溶解后定容为250ml,移取25.00ml此试液,调节pH为9,加入8-羟基喹啉,沉淀Al3+为Al(OC9H6N)3。沉淀经过滤洗涤后,溶于HCl中,加入0.04000mol/LKBrO334.95ml(含过量的KBr),发生如下反应:
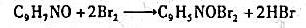
反应完成后,加入过量KI,析出I2,消耗0.1000mo/LNa2S2O3标准溶液20.00ml。计算试样中铝的质量分数。(MAl=26.98)
测定中的其他反应:
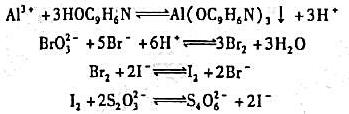
A.称取的重量可为1.5~2.5 g
B.称取的重量可为1.95~2.05 g
C.称取的重量可为1.995~2.005 g
D.称取的重量可为1.9995~2 0005 g
E.称取的重量可为1~3 g
A.取试样一份置105℃±5℃烘箱中烘干至恒重,称取干燥集料试样的总质量,准确至0.1%
B.将试样置一洁净容器中,加入足够数量的洁净水,将集料全部淹没
C.称取每个筛上的筛余量,准确至总质量的0.1%
D.计算各筛分计筛余量及筛底存量的总和与筛分前试样的干燥总质量之比,相差不得超过筛前干燥集料质量的0.5%
E.用搪瓷盘作筛分容器,按筛孔大小排列顺序逐个将集料过筛
锰及其他金属元素,称取127.3mg试样溶解在酸中并加入适当掩蔽剂,以防止其他金属离子的干扰。铁和锰分别以Fe(C9H6NO)3(相对分子质量:488.28) 和Mn(C9H6NO)2(相对分子质量:343.23) 的形式沉淀,共得到沉淀867.8mg,同时用去8-羟基喹啉5.276mmol.试分别计算铁和锰的含量。
称取乙酰水杨酸试样0.5490g,加入50.00ml0.1660mol/L的NaOH煮沸:

过量碱用去27.14mlHCl。
已知1.00mlHCl相当于0.03814gNa2B4O7·10H2O,即滴定度T=0.03814g/ml,求乙酰水杨酸的百分质量分数?用什么指示剂?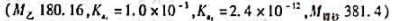
称取含NaCl试样0.5000g,溶解后加入纯AgNO3固体0.8920g,用Fe3+作指示剂,剩余的AgNO3用0.1400mol/L的KSCN溶液回滴,用去23.50ml。求试样中NaCl的质量分数。(试样中除Cl-外,不含有与Ag+生成沉淀的其他物质的离子,MAgNO3=169.9)