 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
结晶时只有同类分子或离子才能排列成晶体,因此结晶具有良好的选择性,利用这种选择性即可实现对混合物的分离。()
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“结晶时只有同类分子或离子才能排列成晶体,因此结晶具有良好的选…”相关的问题
更多“结晶时只有同类分子或离子才能排列成晶体,因此结晶具有良好的选…”相关的问题
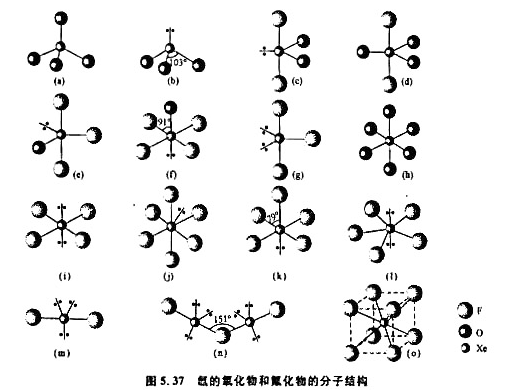
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?
下列说法是否正确?为什么?举例说明.
(1)两个单键就组成一个双键.
(2)非极性分子中只有非极性键.
(3)极性分子中的化学键都有极性.
(4)有共价键的化合物都不可能形成离子晶体.
(5)全由共价键结合的物质只能形成分子晶体.
(6)分子量越大,分子间力越大.
(7)极性分子之间的作用力就是取向力.
(8)色散力仅存在于非极性分子之问.
(9)碘化氢的分子间力比碘化氢大,故碘化氢没有溴化氢稳定.
(10)氢键是一种特殊的分子间力,仅存在于分子之间.
A.机体缺Ca2+或对a2+的需要增加时吸收增加
B.胃酸及维生素C抑制Ca2+的吸收
C.只有离子状态的Ca2+才能被吸收D维生素
D.可促进Ca2+的吸收
E.主要在十二指肠和空肠前段吸收
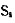 分子既可结晶成单斜硫,也可结晶成正交硫。用X射线行射法(CuKα射线)测得某正交硫晶体的晶胞参数=1048pm,b=1292pm,c=2455pm。已知该硫磺的密度为2.07gcm-3,S的相对原子质量为32.06。
分子既可结晶成单斜硫,也可结晶成正交硫。用X射线行射法(CuKα射线)测得某正交硫晶体的晶胞参数=1048pm,b=1292pm,c=2455pm。已知该硫磺的密度为2.07gcm-3,S的相对原子质量为32.06。
(1)计算每个晶胞中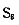 分子的数目;
分子的数目;
(2)计算224衍射线的Bragg角 ;
;
(3)写出气相中 分子的全部独立的对称元素。
分子的全部独立的对称元素。