 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
可逆反应在此温度下当A的解离度为50%时,反应在密闭容器中达到化学平衡,此时系统的总压力p为()
A.#图片1$#
B.#图片2$#
C.#图片3$#
D.#图片4$#
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.#图片1$#
B.#图片2$#
C.#图片3$#
D.#图片4$#
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“可逆反应在此温度下当A的解离度为50%时,反应在密闭容器中达…”相关的问题
更多“可逆反应在此温度下当A的解离度为50%时,反应在密闭容器中达…”相关的问题
在950℃时,可逆反应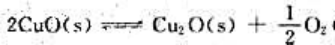 的标准平衡常数
的标准平衡常数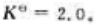 则在此温度下上述反应达到平衡时O2的分压为()。
则在此温度下上述反应达到平衡时O2的分压为()。
A、1.4kPa
B、4.0kPa
C、140kPa
D、400kPa
说明可逆反应的速率常数kt,kt与其平衡常数K之间关系。若已知某温度下氢氟酸解离反应
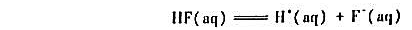
的平衡常数为7.08×10-4mol-1·dm-3,又知基元反应
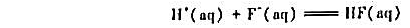
的速率常数为1.00×1011dm3·mol-1·s-1,试求氢氟酸解离反应的速率常数。
已知可逆反应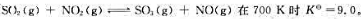 若在此温度下,SO2、NO2、SO2和NO的分压都为50kPa,试通过计算判断反应进行的方向。
若在此温度下,SO2、NO2、SO2和NO的分压都为50kPa,试通过计算判断反应进行的方向。
在373K下,反应:COCI2(g)===CO(g)+Cl2(g)的Kp=8×109,ΔSƟ373=125.5J/K。
计算:(1)373K,总压为202.6kPa时COCl2的解离度;
(2)373K下上述反应的ΔHƟ:
(3)总压为200kPa,COCl2的解离度为0.1%时的温度,设ΔCp=0。
100℃时下列反应的Kθ=8.1×10-9,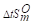 =125.6J·mol·K-1.计算:
=125.6J·mol·K-1.计算:
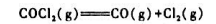
(1)100℃,总压为200KPa时COCl2的解离度;
(2)100℃下上述反应的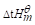 ;
;
(3)总压为200kPa,COCl2的解离度为0.1%时的温度,设ΔTGp,m=0.
已知反应 的标准摩尔焓变
的标准摩尔焓变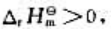 ,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措施是()。
,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措施是()。
A、将系统的体积压缩为原来的1/2
B、体积保持不变,加入惰性气体使压力增大到原来的2倍
C、压力保持不变,加入惰性气体使体积增大到原来的2倍
D、体积保持不变,加入NO气体使压力增大到原来的2倍
A.弱酸性药物,当pH=pKa时,药物主要以分子型药物存在
B.弱酸性药物,当pH>pKa时,药物主要以分子型药物存在
C.弱碱性药物,当pH>pKa时,药物主要以离子型药物存在
D.弱碱性药物,当pH=pKa时,药物主要以分子型药物存在
E.无论是弱酸性药物还是弱碱性药物,当pH=pKa时,分子型药物与离子型药物各占50%