 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25°C时水的离子积KW</sub>=1.008x10-14</sup>,NaOH,HCI和NaCl的Am</sup>m</sub>分别等于0.0248
已知25°C时水的离子积KW=1.008x10-14,NaOH,HCI和NaCl的Amm分别等于0.024811S.m2·mol-1.0.042616S.m2.mol-1和0.012645S.m2.mol-1.
(1)求25°C时纯水的电导率;
(2)利用上述纯水配制AgBr饱和水溶液,测得溶液的电导率k(溶液)=1.664x10-5S.m-1,求AgBr(s)在纯水中的溶解度.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知25°C时水的离子积KW=1.008x10-14,NaO…”相关的问题
更多“已知25°C时水的离子积KW=1.008x10-14,NaO…”相关的问题
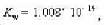 NaOH、HCI和NaCl的
NaOH、HCI和NaCl的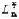 分别等于
分别等于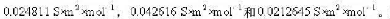 求25°C时纯水的电导率。
求25°C时纯水的电导率。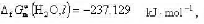 水在25°C时的饱和蒸气压P=3.1663kPa.求25°C时水蒸气的标准摩尔生成吉布斯函数。
水在25°C时的饱和蒸气压P=3.1663kPa.求25°C时水蒸气的标准摩尔生成吉布斯函数。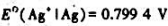 ,
,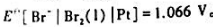 .试计算25℃时
.试计算25℃时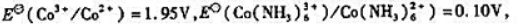
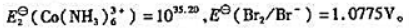
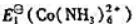 ;
;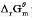 分别为-109.789kJ/mol,77.107kJ/mol和-131.22kJ/mol.求25°C下AgCl(s)在水溶液中的标准溶度积K及溶解度s。
分别为-109.789kJ/mol,77.107kJ/mol和-131.22kJ/mol.求25°C下AgCl(s)在水溶液中的标准溶度积K及溶解度s。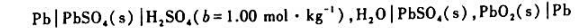
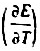 =-4.02x10-4V·K-1.
=-4.02x10-4V·K-1.
















