 更多“由一元弱酸和其共轭碱组成的缓冲溶液,一元弱酸的标准解离常数越…”相关的问题
更多“由一元弱酸和其共轭碱组成的缓冲溶液,一元弱酸的标准解离常数越…”相关的问题
第1题
由一元弱酸和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶
由一元弱酸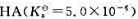 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
第2题
25℃时,一元弱酸HA的标准解离常数则其他共轭碱A的标准解离常数()。0.010mol·l-1.NaA溶液
25℃时,一元弱酸HA的标准解离常数则其他共轭碱A的标准解离常数()。0.010mol·l-1.NaA溶液
点击查看答案
25℃时,一元弱酸HA的标准解离常数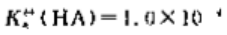
则其他共轭碱A的标准解离常数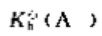 ()。0.010mol·l-1.NaA溶液的pH为()
()。0.010mol·l-1.NaA溶液的pH为()
第3题
对缓冲溶液的正确描述是把一对共轭酸碱联系起来()。
A.缓冲溶液是由一对共轭酸碱组成,且共轭酸、碱间存在质子转移平衡,通过质子H+把一对共轭酸碱联系起来
B.弱酸型缓冲溶液的有效缓冲范围是pH=pKa±1%
C.缓冲溶液加水稀释后,pH几乎不变,缓冲容量也不变
D.某一缓冲溶液200mL的缓冲容量β与该缓冲溶液300mL的缓冲容量β相等
第4题
强碱(酸)滴定一元弱酸(碱),就可以直接准确滴定。如果用K表示滴定反应的形成常数,那么该反应的应
强碱(酸)滴定一元弱酸(碱),就可以直接准确滴定。如果用K表示滴定反应的形成常数,那么该反应的应
点击查看答案
强碱(酸)滴定一元弱酸(碱),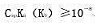 就可以直接准确滴定。如果用K表示滴定反应的形成常数,那么该反应的
就可以直接准确滴定。如果用K表示滴定反应的形成常数,那么该反应的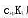 应为多少?
应为多少?
第6题
甲溶液为一元弱酸,其c(H+)=a mol·dm-3,乙溶液为该一元弱酸的钠盐溶液,其c(H+
甲溶液为一元弱酸,其c(H+)=a mol·dm-3,乙溶液为该一元弱酸的钠盐溶液,其c(H+)=b mol·dm-3。当上述甲溶液与乙溶液等体积混合后,测得其c(H+)=c mol·dm-3,试求该一元弱酸的解离平衡常数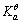 值。
值。
点击查看答案
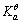 值。
值。
第8题
已知相同浓度的一元弱酸的钠盐NaA、NaB、NaC和NaD的水溶液的pH依次增大,则在下列相同浓度的四种一元弱酸溶液中,一元弱酸的解离度最大的是().
A.HA
B.HB
C.HC
D.HD
第10题
解热镇痛药阿司匹林(乙酰水杨酸)是一元弱酸,其结构式为已知阿司匹林的pH:为3.50,服用后以未解
解热镇痛药阿司匹林(乙酰水杨酸)是一元弱酸,其结构式为已知阿司匹林的pH:为3.50,服用后以未解
点击查看答案
解热镇痛药阿司匹林(乙酰水杨酸)是一元弱酸,其结构式为
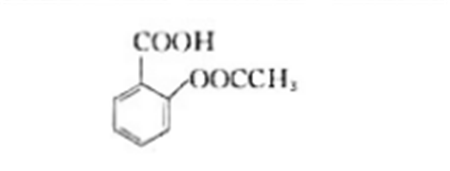 已知阿司匹林的pH:为3.50,服用后以未解离的分子在胃中被吸收。如果患者先吃了调节胃液酸度的药物,使胃液的pH保持在2.95.此时再吃两片阿司匹林(共含0.65g阿司匹林)。假如服用后阿司匹林立即溶解,且不改变胃液的pH,未解离的分子可完全被胃液所吸收,此时能被吸收的阿司匹林有多少克?
已知阿司匹林的pH:为3.50,服用后以未解离的分子在胃中被吸收。如果患者先吃了调节胃液酸度的药物,使胃液的pH保持在2.95.此时再吃两片阿司匹林(共含0.65g阿司匹林)。假如服用后阿司匹林立即溶解,且不改变胃液的pH,未解离的分子可完全被胃液所吸收,此时能被吸收的阿司匹林有多少克?


 如果结果不匹配,请
如果结果不匹配,请 


















