 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
温度为400K,体积为2m3的容器中装有2mol的理想气体A和8mol的理想气体B,则该混合气体中B的分压pB=()kPa.
温度为400K,体积为2m3的容器中装有2mol的理想气体A和8mol的理想气体B,则该混合气体中B的分压pB=()kPa.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“温度为400K,体积为2m3的容器中装有2mol的理想气体A…”相关的问题
更多“温度为400K,体积为2m3的容器中装有2mol的理想气体A…”相关的问题
A.3kg/cm2
B.l.33kg/cm2
C.2.3kg/cm2
D.0.75kg/cm2
在500K时将 在体积为15.0L的容器内达到下列化学平衡:
在体积为15.0L的容器内达到下列化学平衡: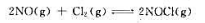 当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的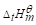
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
(A)最高工作压力为0.05MPa,直径为0.2m且体积为0.1m3介质为气体的容器;
(B)最高工作压力为0.20MPa,直径为0.1m且体积为0.1m3介质为气体的容器;
(C)最高工作压力为0.20MPa,直径为0.2m且体积为0.1m3介质为气体的容器;
(D)最高工作压力为0.50MPa,直径为1m且体积为10m3介质为70℃水的容器。