 更多“下列物质可由金属与盐酸直接反应制取的是()”相关的问题
更多“下列物质可由金属与盐酸直接反应制取的是()”相关的问题
实验室中,常用盐酸与二氧化锰作用制取氯气,如何控制条件使反应MnO2+4HCl→Cl2+MnCl2+2H2O正向进行?为什么?当其他物质均处于标准态时,若反应正向进行,HCl的最低浓度为多大?
A.向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO
B.常温下可用Fe与AgCl反应制取Ag
C.用过量的Cu(OH)2除去CuSO4溶液中的少量H2SO4
D.可分别将Mg、Fe、Cu、Ag放入稀盐酸中,可确定它们的活动性顺序
写出下列过程的反应方程式,并予以配平.
(1)金属镁在空气中燃烧生成两种二元化合物;
(2)在纯氧中加热氧化钡;
(3)氧化钙用来除去火力发电厂排出废气中的二氧化硫;
(4)唯一能生成氮化物的残金属与氮气反应;
(5)在消防队员的空气背包中,超氧化钾既是空气净化剂又是供氧剂;
(6)用硫酸锂同氢氧化钡反应制取氢氧化锟;
(7)镀是s区元索中唯一的两性元素,它与氢氧化钠水溶液反应生成了气体和澄清的溶液;
(8)铍的氢氧化物与氢氧化钠溶液混合;
(9)金属钙在空气中燃烧,将燃烧产物再与水反应.
A.pH大于7的溶液一定是碱溶液
B.质子数相同的原子一定属于同种元素
C.与盐酸反应有气体生成的物质一定是碳酸盐
D.生成两种化合物的反应一定是复分解反应
简要回答下列问题:
(1)电解NaCl熔盐制取金属Na的过程中,为什么要加入CaCl2?由此带来的负面影响是什么?
(2)为什么金属Mg与冷水反应极慢,却可以迅速与热水或NH4Cl水溶液发生反应?
(3)什么是离子势φ?为什么φ的大小可以影响一些氧化物的水化物的解离方式?
(4)为什么加热MgCl2·6H2O时得不到无水盐?
(5)为降低煤炭燃烧时排向大气的SO2量,可以把CaO或CaCO3掺到含硫的煤炭中。试说明这种做法的化学原理,写出相关的化学反应方程式。
(6)Li+和Mg2+半径十分接近,试分析它们的碳酸盐分解温度的高低。
(7)锂的第一电离能比钠大,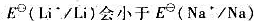 ?既然
?既然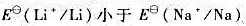 ,为什么锂与水的反应却不如钠剧烈?
,为什么锂与水的反应却不如钠剧烈?
(8)试说明锂的哪些性质与镁相似而有别于钠、钾。
(9)试说明铍的哪些性质与铝相似而有别于镁、钙。
(10)试用价层电子对互斥理论和杂化轨道理论,讨论XeF6分子的几何构型和中心原子的轨道杂化方式。
完成并配平下列化学反应方程式。
(1)在加热条件下金属铈与氯气反应。
(2)金属镧溶于热水。
(3)三氧化二镧溶于硝酸。
(4)三氧化二镝溶于盐酸。
(5)二氧化镨溶于水。
(6)向三氯化镱溶液中滴加氢氧化钠溶液。
(7)金属铀与高温水蒸气反应。
(8)铀溶于盐酸。
(9)高温下氢气还原八氧化三铀。
(10)三氧化铀受热分解。
。向(C)的溶液中通入CO2,有白色沉淀(E)析出,(E)不溶于氨水。在较低的温度下加热(E)有(F)生成,(F)易溶于盐酸,也溶于氢氧化钠溶液。但在高温下灼烧(E)后生成的(G)既不溶于盐酸,也不溶于氢氧化钠溶液。试给出(A),(B),(C),(D),(E),(F)和(G)所代表的物质的化学式,并用化学反应方程式表示各过程。

 如果结果不匹配,请
如果结果不匹配,请 

















