 更多“原子序数为24的元素,其基态原子的价层电子构型应足().”相关的问题
更多“原子序数为24的元素,其基态原子的价层电子构型应足().”相关的问题
第3题
试写出下列元素基态原子的电子排布式,并给出原子序数和元素名称。(1)第4个稀有气体元索;(2)第四周期的第6个过渡元索;(3)4p轨道半充满的元素;(4)电负性最大的元素;(5)4f轨道填充4个电子的元索;(6)第一条4d轨道全充满的元素。
试写出下列元素基态原子的电子排布式,并给出原子序数和元素名称。(1)第4个稀有气体元索;(2)第四周期的第6个过渡元索;(3)4p轨道半充满的元素;(4)电负性最大的元素;(5)4f轨道填充4个电子的元索;(6)第一条4d轨道全充满的元素。
点击查看答案
第4题
下列关于碳族元素说法错误的是()。
A.碳族元素基态原子的价电子层结构为ns2np2
B.锡的金属性质比锗强,可以与非氧化性的酸反应
C.碳酸盐的热稳定性不高主要取决于碳原子的杂化方式
D.硅酸是二元酸,比碳酸还弱
第8题
2019年是元素周期表发明150周年,以下关于周期表中第四周期的第8个元素的说法,错误的是()。
A.处于周期表的第Ⅷ族
B.+3价阳离子的电子构型为[Ar]3d5
C.原子序数为26
D.处于周期表的d区
第9题
乙烯(H2C=CH2)分子中,两个C原子之间成双键。试以左C原子为中心,用价层电子对互斥理论判断其空间构型,并用杂化轨道理论解释其成键情况。
乙烯(H2C=CH2)分子中,两个C原子之间成双键。试以左C原子为中心,用价层电子对互斥理论判断其空间构型,并用杂化轨道理论解释其成键情况。
点击查看答案

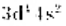
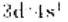
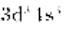
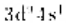

 如果结果不匹配,请
如果结果不匹配,请 

















