 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将铜币置于盛有20 mL 0.1 mol·L-1 AgNO3溶液的烧杯中,可观察到()
A.溶液变红
B.溶液颜色不变
C.铜币表面变色
D.有大量气泡逸出
 答案
答案
C、铜币表面变色
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.溶液变红
B.溶液颜色不变
C.铜币表面变色
D.有大量气泡逸出
 答案
答案
C、铜币表面变色
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将铜币置于盛有20 mL 0.1 mol·L-1 AgNO3…”相关的问题
更多“将铜币置于盛有20 mL 0.1 mol·L-1 AgNO3…”相关的问题
A.0.1 mol·L-1 NaHCO3溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(碳酸根)>c(碳酸氢根)>c(OH-)
B.20 mL 0.1 mol·L-1 CH3COONa溶液与10 mL 0.1 mol·L-1 HCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(铵根)>c(OH-)
D.0.1 mol·L-1 CH3COOH溶液与0.1 mol·L-1 NaOH溶液 等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH)
A.①②③④⑤
B.④①③②⑤
C.⑤④②①③
D.④③⑤②①
A.②④①⑤③⑥
B.④②①⑤③⑥
C.④②⑤①③⑥
D.②④⑤①③⑥
A.①→②→③→④
B.①→③→②→④
C.①→②→④→③
D.①→④→②→③
现有同体积的四种溶液 (1)0.01 m01·L-1NH4C1—0.01 mol·L-1 NH3 (2)0.1 m01·L-1NH4Cl—0.1 mol·L-1 NH3 (3)0.01 mol·L-1HAc—0.01 mol.L-1 NaAc (4)0.1 mol·L-1HAc—0.1 mol·L-1 NH3 分别加入0.05 mL,1 mol·L-1HAc,引起pH值变化最大的是()。
A.(2)
B.(4)
C.(1)和(3)
D.(2)和(4)
A.100 mL
B.200 mL
C.300 mL
D.400 mL
A.100mL、100 mL
B.400 mL、400 mL
C.100 mL、400 mL
D.400 mL、100 mL
今有一PbO-PbO2混合物,现称取试样1.234g,加入20.00 mL 0.2500mol·L-1草酸溶液将PbO2还原为Pb2+,然后用氨中和,这时Pb2+以PbC2O4形式沉淀,过滤,滤液酸化后用KMnO4滴定,消耗0.04000 mol·L-1KMnO4溶液10.00mL,沉淀溶解于酸中,滴定时消耗0.04000 mol·L-1KMnO4溶液30.00mL.计算试样中PbO和PbO2的质量分数.
(1)写出原电池符号、电池反应式;
(2)查标准电极电势表,求该原电池的标准电动势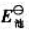 ;
;
(3)当电池反应进行到c(Cu2+)=1.0mol·dm-3时,试计算原电池的电动势E池。
A.配制1 L 0.1 mol·L-1 NaCl溶液的实验中,用托盘天平称取5.85 g NaCl固体
B.用玻璃棒蘸取CH3COOH溶液点在用水润湿的pH试纸上测定该溶液的pH
C.用酸式滴定管量取25.00 mL高锰酸钾溶液
D.可用过滤的方法除去淀粉溶液中混有的少量NaCl杂质