 更多“我能写出羟基酸发生缩聚反应方程式()”相关的问题
更多“我能写出羟基酸发生缩聚反应方程式()”相关的问题
判断下列反应过程能否实现,写出有关的化学反应方程式。
①硼酸与氨水发生酸碱中和反应;
②三氯化铊与硫化钠反应生成Tl2S3;
③Al(NO3)3与Na2CO3作用生成Al2(CO3)3沉淀;
④铝酸钠与NH4Cl反应生成铝酸铵。
高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH 主要的生产流程如下: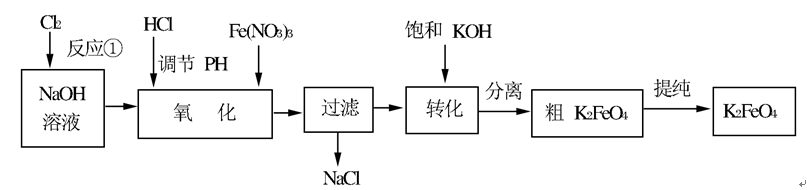 问题一、写出反应①的离子方程式()。
问题一、写出反应①的离子方程式()。
问题二、流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4)()Ksp(Na2FeO4)〔填“>”或“<”或“=”〕。
问题三、反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最正确时,NaClO浓度对K2FeO4生成率的影响
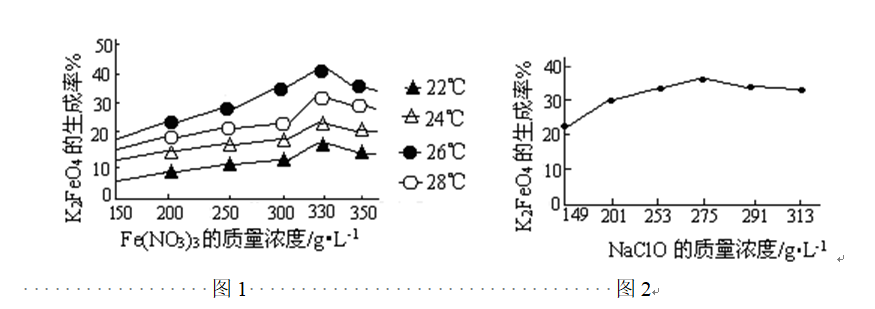
①工业生产中最正确温度为()℃,此时Fe(NO3)3与NaClO两种溶液最正确质量浓度之比为()。
②假设NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:()。假设Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化复原反应生成K3FeO4,此反应的离子方程式:()。
问题四、K2FeO4在水溶液中易水解:
4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
AH2O
BCH3COONa、异丙醇
CNH4Cl、异丙醇
DFe(NO3)3、异丙醇
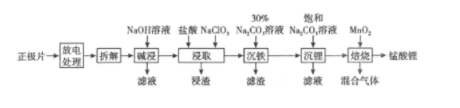 以废旧磷酸亚铁锂电池正极片(LiFePO4炭黑和铝箔等)为原料制备锰酸锂(LiMn2O4)的流程如图所示。回答下列问题:
以废旧磷酸亚铁锂电池正极片(LiFePO4炭黑和铝箔等)为原料制备锰酸锂(LiMn2O4)的流程如图所示。回答下列问题:
问题1、LiFePO4中Fe元素的化合价为;“放电处理”有利于锂在正极的回收,其原因是()。
问题2、“碱浸”中发生反应的离子方程式为()。
问题3、“浸取”中加入NaClO3的作用为;“沉铁”过程所得滤渣为白色固体,其主要成分是()。
问题4、已知碳酸锂的分解温度为723℃。当“焙烧”温度达到515℃时,开始有CO2产生,可能的原因是;MnO2可以利用MnSO4溶液与K2S2O8溶液反应制备,该反应中氧化剂与还原剂的物质的量之比为()。
问题5、写出“焙烧”过程中生成锰酸锂的化学方程式。


 如果结果不匹配,请
如果结果不匹配,请 

















