 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知N2的平衡解离能=955.42kJmol-1,其基本振动波数为2330cm-1,计算光谱解离能D0
已知N2的平衡解离能 =955.42kJmol-1,其基本振动波数为2330cm-1,计算光谱解离能D0值。
=955.42kJmol-1,其基本振动波数为2330cm-1,计算光谱解离能D0值。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知N2的平衡解离能 =955.42kJmol-1,其基本振动波数为2330cm-1,计算光谱解离能D0值。
=955.42kJmol-1,其基本振动波数为2330cm-1,计算光谱解离能D0值。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知N2的平衡解离能=955.42kJmol-1,其基本振动…”相关的问题
更多“已知N2的平衡解离能=955.42kJmol-1,其基本振动…”相关的问题
H2,N2与100g水在40℃时处于平衡、平衡总用为105.4kPa.平衡气体经干燥后的体积分数 =0.40.假设溶液的水蒸气压等于纯水的饱和蒸气压,即40℃时的7.33WPa.已知40℃时H2,N2在水中的宁利系数分别为7.61Gpa及10.5GPa,求40℃时水中能溶解H2,N2的质量.
=0.40.假设溶液的水蒸气压等于纯水的饱和蒸气压,即40℃时的7.33WPa.已知40℃时H2,N2在水中的宁利系数分别为7.61Gpa及10.5GPa,求40℃时水中能溶解H2,N2的质量.
已知298.15K时,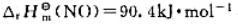 ,反应N2(g)+O2(g)=2NO(g)的
,反应N2(g)+O2(g)=2NO(g)的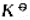 =4.5×10-31。
=4.5×10-31。
(1)计算500K时该反应的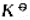 ;
;
(2)汽车内燃机中汽油的燃烧温度可达1575K,根据平衡移动原理说明该温度是否有利于NO的生成。
在77.2K时,用微球型硅酸铝催化剂吸附N2(g),在不同的平衡压力下,测得每千克催化剂吸附的N2(g)在标准状况下的体积数据如下:

已知77.2K时N2(g)的饱和蒸气压为99.125kPa,每个N2分子的截面积a=16.2x10-20m2.
试用BET公式计算该催化剂的比表面积.
根据下列已知数据,由玻恩-哈伯循环计算氯化钡的 。
。
氯分子的解离能 242.6 kJ·mol-1
钡的原子化热177.8 kJ·mol-1
钡的第一电离能550.9 kJ·mol-¿105 106¿
钡的第二电离能962.3 kJ·mol-1
氯的电子亲和能348.6 kJ·mol-1
氯化钡的晶格能2026.7 kJ·mol-1
A.(M1,N2)
B.(M2,N1)
C.(M2,N2)
D.(M1,N1)
反应N2(g)+3H2(g)=2NH3(g)(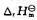 >0)达到平衡后采取下列哪种方法能使平衡向有移动。()
>0)达到平衡后采取下列哪种方法能使平衡向有移动。()
A.加入催化剂
B.降低温度
C.增加H2的压力
D.降低系统的总压
A.低温低压
B.低温高压
C.高温高压
D.高温低压