 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
可逆反应N2O4(g)2NO2(g)在628K时标准平衡常数为1.00。分别计算N2O4的压力为400kPa和1000kPa时N2O4的平衡转化率,并解释计算结果。
可逆反应N2O4(g)2NO2(g)在628K时标准平衡常数为1.00。分别计算N2O4的压力为400kPa和1000kPa时N2O4的平衡转化率,并解释计算结果。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“可逆反应N2O4(g)2NO2(g)在628K时标准平衡常数…”相关的问题
更多“可逆反应N2O4(g)2NO2(g)在628K时标准平衡常数…”相关的问题
306K时,反应N2O4(g)=2NO2(g)的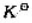 =0.26.在容积为10L的容器中加入4.0molN2O4和1.0molNO2,则开始时p(总)=()kPa,反应向()方向进行。
=0.26.在容积为10L的容器中加入4.0molN2O4和1.0molNO2,则开始时p(总)=()kPa,反应向()方向进行。
当NO2被冷却到室温时,发生聚合反应:
2NO2(g)→N2O4(g)
若在高温下将15.2gNO2充入10.0L的容器中,然后使其冷却到25℃.测得总压为0.500atm.
试计算NO2(g)和N2O4(g)的摩尔分数的关系即可求解.
 则反应开始前p总=(),反应进行的方向是().
则反应开始前p总=(),反应进行的方向是().
A.CO(g)+Cl2(g)→COCl2(g)
B.2NO2(g)→NO(g)+1/2O2(g)
C.N2(g)+O2(g)→2NO(g)
D.NH4HS(s)→NH3(g)+H2S(g)
A.升温加压
B.升温降压
C.降温加压
D.降温降压
O(1),写出有关反应式,利用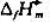 数据计算N2H4(1)的摩尔燃烧热.
数据计算N2H4(1)的摩尔燃烧热.