 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应2NO(g)+O2(g)==2NO2(g)的ΔrHm<0,当上述反应达平衡后,若要使平衡向产物方向移动,可以采取措施为()。
A.升温
B.减压
C.添加惰性气体
D.降温
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.升温
B.减压
C.添加惰性气体
D.降温
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应2NO(g)+O2(g)==2NO2(g)的ΔrHm…”相关的问题
更多“已知反应2NO(g)+O2(g)==2NO2(g)的ΔrHm…”相关的问题
已知298.15K时,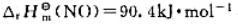 ,反应N2(g)+O2(g)=2NO(g)的
,反应N2(g)+O2(g)=2NO(g)的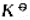 =4.5×10-31。
=4.5×10-31。
(1)计算500K时该反应的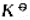 ;
;
(2)汽车内燃机中汽油的燃烧温度可达1575K,根据平衡移动原理说明该温度是否有利于NO的生成。
一定条件下反应2NO(g)+O2(g) 2NO2(g)达到平衡.已知该反应的
2NO2(g)达到平衡.已知该反应的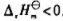 .若保持温度不变、增大压力,则平衡();若保持温度、体积不变,加入惰性组分,则平衡();若保持压力不变、降低温度,则平衡().(选择填入:向左移动、向右移动、不发生移动.)
.若保持温度不变、增大压力,则平衡();若保持温度、体积不变,加入惰性组分,则平衡();若保持压力不变、降低温度,则平衡().(选择填入:向左移动、向右移动、不发生移动.)
二氧化氮的分解反应2NO(g)→+2NO(g)+O2(g),319℃时,k1=0.498mol·L-1.
s-1;354℃时,k2=1.81mol·L-1.s-1.计算该反应的活化能E.和指前参最k0以及383℃时反应速率常数k.
A.升温加压
B.升温降压
C.降温加压
D.降温降压
2NO2(g).25℃下该反应的初始速率实验数据如表3-1:

(1)写出反应速率方程;
(2)计算25℃时反应速度系数k;
(3)co(NO)=0.0030mol·L-2,co(O2)=0.0015rmol·L-2时,相应的初始速半为多少?
A.0.03mol·Lˉ1·sˉ1
B.0.015mol·Lˉ1·sˉ1
C.0.12mol·Lˉ1·sˉ1
D.0.06mol·Lˉ1·sˉ1
已知下列两个反应:
(1)2H2(g)+O2(g)=2H2O(1);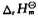 (298K)=-571.70kJ·mol-1
(298K)=-571.70kJ·mol-1
(2)2H2(g)+O2(g)=2H2O(g);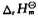 (298K)=-483.65kJ· mol-1
(298K)=-483.65kJ· mol-1
求298K时水的标准摩尔汽化热。
已知
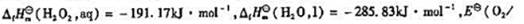
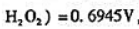
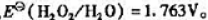
试计算25℃时反应2H2O2(I)→2H2O(l)+O2(g)的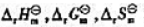 和标准平衡常数Kθ.
和标准平衡常数Kθ.
反应2SO2(g)+O2(g) 2SO3(g)在1000K时的KƟ=3.4×10-5,计算1100K时的KƟ。已知该反应的ΔrHƟm=-189kJ/mol,并设在此温度范围内ΔrHƟm只为常数。
2SO3(g)在1000K时的KƟ=3.4×10-5,计算1100K时的KƟ。已知该反应的ΔrHƟm=-189kJ/mol,并设在此温度范围内ΔrHƟm只为常数。