 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取粗铵盐1.075g,与过量碱共热,蒸出的NH3以过量硼酸溶液吸收,再以0.3865mol·L-1HCI滴定至甲基红和溴甲酚绿混合指示剂终点,需33.68mLHCI溶液,求试样中NH3的质量分数和以NH4Cl表示的质量分数.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“称取粗铵盐1.075g,与过量碱共热,蒸出的NH3以过量硼酸…”相关的问题
更多“称取粗铵盐1.075g,与过量碱共热,蒸出的NH3以过量硼酸…”相关的问题
称取乙酰水杨酸试样0.5490g,加入50.00ml0.1660mol/L的NaOH煮沸:

过量碱用去27.14mlHCl。
已知1.00mlHCl相当于0.03814gNa2B4O7·10H2O,即滴定度T=0.03814g/ml,求乙酰水杨酸的百分质量分数?用什么指示剂?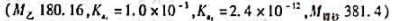
放冷,移置250ml量瓶中,加入K2Cr2O7滴定液(0.01600mol/L)50ml,加水稀释至刻度,振摇5分钟,用干燥滤纸滤过,精密量取续滤液100ml,置250ml碘瓶中,加过量KI和HCl溶液(1→2)10ml,密封,摇匀,在暗处放置10分钟后,用Na2S2O3滴定液(0.1002mol/L)滴定至终点,用去11.26ml。①求1ml重铬酸钾滴定液(0.01600mol/L)相当于盐酸小檗碱的质量;②按干燥品计算盐酸小檗碱的质量分数。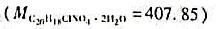
A.利用指示剂共轭酸式共碱式颜色不同
B.利用指示剂本身与指示剂待测离子形成的配离子颜色不同
C.利用指示剂氧化型还原型颜色不同
D.利用指示剂氧化型还原型电极电位不同
E.利用指示剂与过量的滴定剂生成有色沉淀
Na2S2O3溶液滴定.计算试样中KI的质量分数.
用化学反应方程式表示下列过程:
(1)在加热条件下氯气分别与金属铬、镉、银作用。
(2)氯气和氢气的混合物被强光照射。
(3)单质碘和氢气的混合物共热。
(4)高温下氯气与单质硅反应。
(5)过量氯气与单质磷在四氯化碳溶液中反应。
(6)碘在碱溶液中歧化。
(7)将浓盐酸滴加到固体高锰酸钾上。
(8)碘化钠与二氧化锰在硫酸介质中反应。
(9)溴化钠与浓硫酸作用。
(10)氢氟酸与二氧化硅作用。
(11)氟化钙、氯化钠分别与热浓硫酸作用。
(12)氢碘酸在常温下被空气中的氧气所氧化。
(13)把液态溴滴到红磷和少许水的混合物上。
(14)将水滴到红磷与单质碘的混合物上。
(15)金属锌、氧化铜、氢氧化钠、碳酸钙分别与稀盐酸作用。
(16)单质碘与氯气在碱性介质中反应。
(17)氟气和氯气在高温下反应。
(18)将氟化银溶于三氟化溴中。
(19)次氯酸分别在下面几种条件下分解:
①光照;②受热;③有干燥剂。
(20)亚氯酸的歧化分解。
(21)将二氧化氯通人过氧化钠溶液中。
(22)氯酸在下面两种条件下分解:
①光照;②受热歧化。
(23)溴酸钠与二氟化氙作用。
A.①
B.②
C.③
D.④