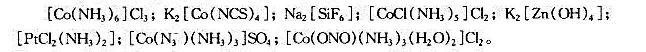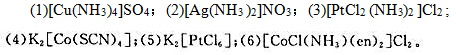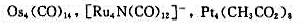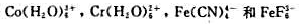题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
指出下列配合物的中心离子及价数、配位体及配位数、配合离子的电荷和配合物名称: (1)K2[PtCl6];(2
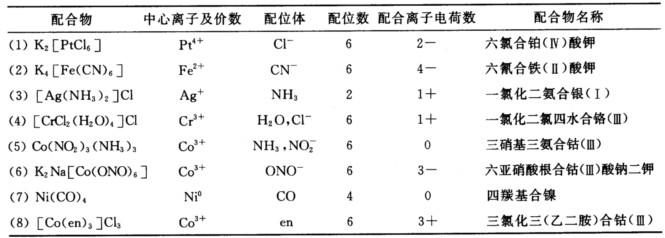
指出下列配合物的中心离子及价数、配位体及配位数、配合离子的电荷和配合物名称: (1)K2[PtCl6];(2)K4[Fe(CN)6];(3)[Ag(NH3) 2]Cl;(4)[CrCl2 (H2O)4]Cl; (5)[Co(NO2) 3 (NH3) 3];(6)K2Na[Co(ONO) 6];(7)Ni(CO) 4;(8)[Co(en) 3]Cl3。
 答案
答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“指出下列配合物的中心离子及价数、配位体及配位数、配合离子的电…”相关的问题
更多“指出下列配合物的中心离子及价数、配位体及配位数、配合离子的电…”相关的问题