题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试写出下列各电池的电极反应和电池反应。 (1)Cu(s)|CuSO4(a1)||AgNO3(a2)|Ag(s) (2)Pb(s)|PbSO4
试写出下列各电池的电极反应和电池反应。 (1)Cu(s)|CuSO4(a1)||AgNO3(a2)|Ag(s) (2)Pb(s)|PbSO4(s)|K2SO4(a1)||HCl(a2)|AgCl(s)|Ag(s) (3)Pt|H2(P)|NaOH(a)|HgO(s)|Hg(1) (4)Pt|H2(P1)|H2SO4(m)|H2(P2)|Pt (5)K(Hg)(a1)|K+(a2)||Cl-(a3)|Hg2Cl2(s)|Hg(1)
 答案
答案
(1)电极反应和电池反应分别为
负极 Cu(s)→Cu2+(1)+2e-
正极 2Ag+(a2)+2e-→2Ag(s)
电池反应Cu(s)+2Ag+(a2)→cu2+(a1)+2Ag(s)
(2)电极反应和电池反应分别为
负极Pb(s)+SO42-(a1)→PbSO4(s)+2e-
正极 2AgCl(s)+2e-→Ag(s)+2Cl-(a2)
电池反应Pb(s)+SO42-(a1)+2AgCl(s)→PbSO4(s)+2Ag(s)+2Cl-(a2)
(3)电极反应和电池反应分别为
负极 H2(p)+2OH-(a)→H2O+2e-
正极 HgO(s)+H2O+2e-→Hg(l)+2OH-(a)
电池反应HgO(s)+H2(p)→Hg(l)+H2O(l)
(4)电极反应和电池反应分别为
负极 H2(p1)→2H+(m)+2e-
正极 2H+(m)+2e-→H2(p2)
电池反应 H2(p1)→H2(p2)
(5)电极反应和电池反应分别为
负极 2K(Hg)(a1)→2K+(a2)+2Hg(l)+2e-
正极 Hg2Cl2(s)+2e→+2Hg(l)
电池反应 2K(Hg)+Hg2Cl2(s)→2K+(a2)+2Cl-(a3)+4Hg(l)
(1)电极反应和电池反应分别为负极Cu(s)→Cu2+(1)+2e-正极2Ag+(a2)+2e-→2Ag(s)电池反应Cu(s)+2Ag+(a2)→cu2+(a1)+2Ag(s)(2)电极反应和电池反应分别为负极Pb(s)+SO42-(a1)→PbSO4(s)+2e-正极2AgCl(s)+2e-→Ag(s)+2Cl-(a2)电池反应Pb(s)+SO42-(a1)+2AgCl(s)→PbSO4(s)+2Ag(s)+2Cl-(a2)(3)电极反应和电池反应分别为负极H2(p)+2OH-(a)→H2O+2e-正极HgO(s)+H2O+2e-→Hg(l)+2OH-(a)电池反应HgO(s)+H2(p)→Hg(l)+H2O(l)(4)电极反应和电池反应分别为负极H2(p1)→2H+(m)+2e-正极2H+(m)+2e-→H2(p2)电池反应H2(p1)→H2(p2)(5)电极反应和电池反应分别为负极2K(Hg)(a1)→2K+(a2)+2Hg(l)+2e-正极Hg2Cl2(s)+2e→+2Hg(l)电池反应2K(Hg)+Hg2Cl2(s)→2K+(a2)+2Cl-(a3)+4Hg(l)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“试写出下列各电池的电极反应和电池反应。 (1)Cu(s)|C…”相关的问题
更多“试写出下列各电池的电极反应和电池反应。 (1)Cu(s)|C…”相关的问题
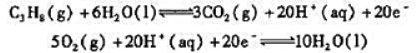
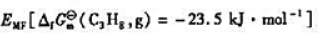
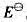 。
。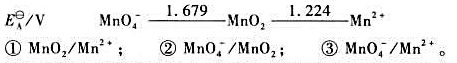
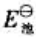 和电池反应的
和电池反应的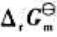 。
。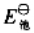 和电池反应的
和电池反应的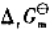 。
。 ;
;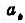 和
和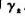 .
.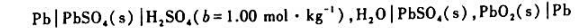
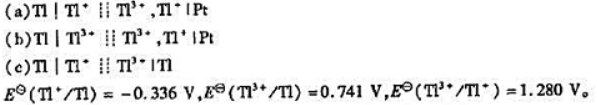
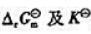 .
. ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。
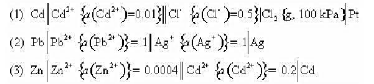
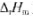 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为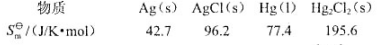 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数